
Научная электронная библиотека
Монографии, изданные в издательстве Российской Академии Естествознания

Сологуб Т. В., Романцова М. Г., Кремень Н. В., Александрова Л. М., Аникина О. В., Суханов Д. С., Коваленко А. Л., Петров А. Ю., Ледванов М. Ю., Стукова Н. Ю., Чеснокова Н. П., Бизенкова М. Н., Понукалина Е. В., Невважай Т. А.,
2.2.4. Сравнительная оценка антиоксидантных свойств цитофлавина и неотона при экспериментальном ишемическом повреждении миокарда
Активация липопероксидации - типовой процесс дезинтеграции биологических мембран при различных формах патологии инфекционной и неинфекционной природы, сопровождающихся гипоксией.
Как известно, независимо от характера индуктора ключевую роль в развитии окислительного повреждения клеток играют активные формы кислорода, органические радикалы и перекиси. Активные формы кислорода могут образовываться интрацеллюлярно в сфере действия оксидазных энзимов, а также экстрацеллюлярно - при участии лейкоцитов. Большая часть молекул кислорода, попавших в клетку, подвергается ферментативному катаболизму в митохондриях в процессе двух - и тетраэлектронного восстановления, катализируемого цитохромоксидазой. Однако в условиях дефицита кислорода возникает ступенчатое одноэлектронное восстановление молекулярного кислорода с образованием свободных радикалов и последующими цепными реакциями свободнорадикального перекисного окисления липидов (ПОЛ), белков, нуклеиновых кислот и углеводов [13].
В связи с вышеизложенным становиться очевидным, что активация процессов липопероксидации является важнейшим звеном дестабилизации мембран миокардиоцитов при ишемической болезни сердца (ИБС). Активация ПОЛ сопровождается модификацией состава и структуры липопротеидных комплексов клеточных мембран, а также активности связанных с мембраной ферментных систем, нарушением трансмембранного переноса ионов, электролитного баланса клеток и их возбудимости. Одновременно возникает утрата мембранных рецепторов и соответственно нарушение гуморального и нервного контроля за внутриклеточной метаболической активностью миокарда [36].
Обращает на себя внимание тот факт, что активация процессов липопероксидации в миокарде возникает не только в условиях ишемии, но при реперфузии миокарда после длительной ишемии. Усиление притока крови, богатой кислородом, в ранее ишемизированный миокард сопровождается активацией липопероксидации на фоне недостаточности ферментного звена антиоксидантной системы (АОС), избыточного поступления Са2+ через мембраны ишемизированных миокардиоцитов. Одновременно возникает потеря К+ миокардиоцитами, что приводит к развитию реперфузионных аритмий [36].
Как известно, ранним признаком повреждения тканей при ишемии миокарда, оксидативном стрессе, реперфузионном синдроме, атеросклерозе и других патологиях является окислительная модификация белков [13].
Под влиянием АФК возникает сбрасывание белковых рецепторных компонентов мембран, так называемый шеддинг, что приводит к нарушению нервной и гуморальной регуляции функциональной активности миокардиоцитов [41, 49].
В настоящее время очевидна корреляционная взаимосвязь между интенсификацией свободнорадикальных процессов, в частности, перекисным окислением липидов (ПОЛ), дестабилизацией биологических мембран клеток различных органов, активацией внешнего, внутреннего, альтернативного механизмов формирования протромбиназы, тромбоцитарного звена системы гемостаза, нарушениями коагуляционного потенциала и реологических свойств крови. Естественно, что активация свободнорадикального окисления при ишемическом повреждении миокарда, являясь одним из эфферентных звеньев развития альтерации и некроза миокардиоцитов, потенцирует инициирующие механизмы формирования коронарной недостаточности за счет длительной индукции тромбообразования с последующим возможным развитием ДВС - синдрома [13, 36, 41, 49].
Вышеизложенное делает очевидным целесообразность дальнейшего поиска лекарственных препаратов, обеспечивающих реактивацию ферментного звена АОС крови и тканей, и соответственно подавление избыточного образования свободных радикалов.
В последние годы в клинической и экспериментальной медицине широкое распространение получили такие антигипоксанты и антиоксиданты, как реамберин, цитофлавин, атмизол-сукцинат, ГАМК, коэнзим-Q (убихинон), цитохром С, олифен и др. [2, 8, 9, 11, 23, 26]. Ведущее место по эффективности воздействия на фоне развития тканевой гипоксии занимают, так называемые субстратные антигипоксанты, среди них аспарагиновая, глутаминовая кислоты и их соли, цистеин, АТФ, креатинфосфат, соли янтарной кислоты [30, 44, 47].
До настоящего момента остается малоизученным вопрос о возможности использования макроэргических соединений, в частности, АТФ и креатинфосфата в комплексной терапии ИБС в качестве антигипоксантов и мембранопротекторов.
Целью настоящего исследования явилось изучение влияния цитофлавина и неотона на метаболические сдвиги в ишемизированном миокарде для выявления их новых биологических эффектов как антиоксидантов и мембранопротекторов.
Эксперименты проведены на 60 беспородных крысах - самцах массой 250-300г. Моделирование ишемии и инфаркта миокарда проводили в условиях острого опыта по методу Н.Selye (окклюзия нисходящей ветви левой коронарной артерии на уровне нижнего края ушка) [43, 55]. Одновременно проводили морфологическую и гистохимическую оценку состояния миокарда.
О состоянии антиоксидантной системы судили по уровню активности супероксиддисмутазы (СОД) [16], каталазы [24], а также по уровню восстановленного глутатиона [16, 41] крови и гомогенатов миокарда. Об интенсивности процессов липопероксидации свидетельствовала динамика содержания диеновых конъюгатов (ДК) [54] и малонового диальдегида (МДА) [47] в крови и гомогенатах миокарда на фоне развития острой ишемии миокарда.
Сравнительная оценка состояния липопероксидации и активности АОС крови и тканей проведена в следующих группах наблюдения:
- интактные животные;
- в группе животных с экспериментальной ишемией без медикаментозной коррекции;
- в группе животных с экспериментальной ишемией миокарда и медикаментозной коррекцией, достигаемой внутривенным введением цитофлавина сразу после окклюзии коронарной артерии в дозе 1.5 мл/кг;
- в группе животных с экспериментальной ишемией изучены те же процессы на фоне внутривенного введения неотона в суточной дозе 150мг/кг сразу после окклюзии коронарной артерии далее 1 раз в сутки.
Терапевтический эффект препарата изучали в динамике спустя 60 мин и 72 часа после окклюзии.
Как показали результаты проведенных нами исследований, спустя 60 мин. с момента развития ишемии имело место резкое возрастание уровня МДА (р<0.001) в миокарде. Одновременно отмечалось и увеличение содержания МДА (р<0.001) в сыворотке крови. При этом уровень ДК (р<0.001) в крови не отличался от показателей группы контрольных интактных животных. Спустя 72 часа с момента развития ишемии уровень МДА (р<0.001) в миокарде несколько снижался по сравнению с таковыми показателями в предшествующий период наблюдения (60 мин с момента развития ишемии), но в то же время оставался выше показателей группы интактных контрольных животных. Содержание МДА (р<0.001) в сыворотке крови спустя 72 часа с момента развития ишемии также оставалось значительно выше показателей контроля, но в то же время несколько снижалось по сравнению с ранним периодом острой ишемии миокарда. Уровень ДК (р<0.001) в крови оставался без изменений в течение всего периода наблюдений.
Таким образом, выявление параллелизма между уровнем МДА миокарда и сыворотки крови в динамике острой ишемии миокарда свидетельствует о том, что показатель содержания МДА в крови может быть одним из объективных критериев оценки развития ишемии миокарда, наряду с общепринятыми показателями тестирования инфаркта миокарда по уровню трансаминаз сыворотки крови. Содержание ДК в крови при ишемии миокарда практически не изменяется и не может быть использовано для оценки степени структурных изменений в ишемизированном миокарде.
Одним из патогенетических факторов активации процессов липопероксидации в условиях ишемии может явиться недостаточность антиоксидантной системы крови и тканей. Для частичного решения этого вопроса проведены сравнительные серии экспериментов по установлению корреляционной взаимосвязи состояний активности СОД, каталазы, восстановленного глутатиона сыворотки крови и гомогенатов миокарда в динамике острой ишемии.
Как показали результаты проведенных экспериментов, спустя 60 мин. с момента развития ишемии отмечалось снижение активности СОД (р<0.001) гомогенатов миокарда, между тем активность СОД (р<0.001) сыворотки крови возрастала по сравнению с таковыми показателями группы контроля. Спустя 72 часа с момента развития ишемии активность СОД (р<0.001) гомогенатов миокарда оставалась сниженной, как и в предыдущей группе наблюдения. Одновременно резко снижалась активность СОД (р<0.001) сыворотки крови как по сравнению с таковыми показателями группы животных с ранней стадией острой гипоксии, так и по отношению к показателям контрольной группы животных.
Что касается активности другого фермента - каталазы в динамике ишемии миокарда, следует отметить стабильное снижение ее активности в ранние и поздние сроки наблюдения в гомогенатах миокарда (р<0.001).
Содержание восстановленого глутатиона в гомогенатах миокарда также заметно снижалось уже спустя 60 мин с момента развития острой ишемии миокарда (р<0.001) и оставалось низким спустя 72 часа (р<0.001). Одновременно имело место снижение содержания восстановленного глутатиона и в сыворотке крови экспериментальных животных (р<0.001).
Касаясь значимости выявленного нами феномена, следует отметить, что снижение активности СОД и каталазы в ишемизированном миокарде приводит к дальнейшему избыточному накоплению супероксидного анион-радикала и перекиси водорода, депрессии участков генома, ответственных за активность внутриклеточных ферментативных антиоксидантных систем, например, гена, ответственного за синтез СОД, локализованного в 21 хромосоме.
Под влиянием активных форм кислорода и активации процессов липопероксидации возникает дестабилизация мембран миокардиоцитов, нарушение трансмембранного переноса ионов, аминокислот, глюкозы, с последующим нарушением трофики, электрогенеза, возбудимости и функциональной активности клеток.
В задачи последующих наблюдений входила оценка влияния цитофлавина на состояние процессов липопероксидации и АОС в ишемизированном миокарде.
Как оказалось, в экспериментах с использованием медикаментозной коррекции, применение цитофлавина в значительной мере подавляло чрезмерную интенсификацию процессов липопероксидации как в ранний период наблюдения (60 мин с момента развития ишемии), так и спустя 72 часа с момента развития ишемии. Так, спустя 60 мин с момента развития ишемии имело место заметное снижение уровня МДА в гомогенатах миокарда (р<0.001) и в сыворотке крови (р<0.001). Спустя 72 часа с момента развития ишемии на фоне введения цитофлавина возникало еще более выраженное снижение МДА в гомогенатах миокарда и сыворотке крови по отношению к таковым показателям группы сравнения (р<0.001, рис. 5). Причем в сыворотке крови уровень МДА нормализовался, а в миокарде почти достигал показателей нормы. Обращает на себя внимание тот факт, что уровень ДК (р<0.001) не изменялся в сыворотке крови в динамике ишемии миокарда в обеих группах наблюдения: с применением цитофлавина и без медикаментозной коррекции.
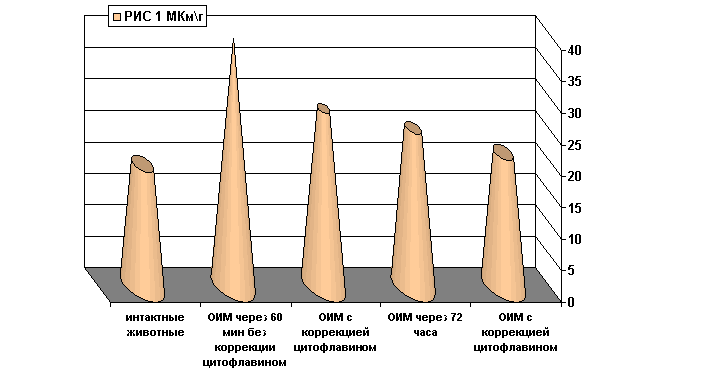
Рисунок 5. Содержание МДА гомогенатов миокарда в условиях острой ишемии миокарда с медикаментозной коррекцией цитофлавином
Примечание: ОИМ - острая ишемия миокарда через 60 мин и 72 часа с момента развития ишемии миокарда. Степень достоверности полученных данных указаны в тексте.
Как показали дальнейшие исследования, в основе снижения содержания в крови и миокарде продуктов липопероксидации на фоне введения цитофлавина лежит активация ферментного звена антиоксидантной системы.
Спустя 60 мин с момента развития ишемии на фоне введения цитофлавина отмечалось повышение активности СОД (р<0.001) и каталазы (р<0.001) гомогенатов миокарда, заметно возрастал уровень восстановленного глутатиона (р<0.001) в миокарде. В то же время активность СОД (р<0.001), каталазы (р<0.001) и уровень восстановленного глутатиона (р<0.001) сыворотки крови не изменялись по отношению к соответствующим показателям группы ишемизированных животных без медикаментозной коррекции.
Спустя 72 часа с момента развития ишемии на фоне введения цитофлавина имело место возрастание и нормализация активности СОД (р<0.001) и каталазы (р<0.001), а также уровня восстановленного глутатиона (р<0.001) в миокарде по сравнению с таковыми показателями группы ишемизированных животных без медикаментозной коррекции. В эти же сроки наблюдения под влиянием цитофлавина достоверно возрастала активность СОД (р<0.001), каталазы (р<0.001), уровень восстановленного глутатиона (р<0.001) в сыворотке крови.
Результаты проведенных исследований позволили сделать следующие выводы:
- 1. Ведущим патогенетическим фактором повреждения ишемизированного миокарда является активация процессов липопероксидации, сочетающаяся с недостаточностью ферментного звена антиоксидантной системы крови и миокарда, а также с дефицитом восстановленного глутатиона.
- 2. Выявлена корреляция между возрастанием уровня МДА и снижением восстановленного глутатиона в гомогенатах ишемизированного миокарда и сыворотке крови. Мониторинг указанных показателей в сыворотке крови может быть использован в качестве объективных критериев оценки развития деструктивных процессов в миокарде.
- 3. Достигнута реактивация СОД и каталазы гомогенатов миокарда и сыворотки крови в динамике экспериментальной ишемии миокарда при использовании цитофлавина.
Резюмируя полученные данные в целом, следует заключить, что использование цитофлавина в группе животных с экспериментальной ишемией миокарда оказывает положительные метаболические эффекты в виде активации ферментного звена АОС гомогенатов миокарда и сыворотки крови при одновременном снижении содержания промежуточных продуктов липопероксидации.
В связи с этим, цитофлавин - препарат, обладающий свойствами антиоксиданта, антигипоксанта, мембранопротектора за счет содержащихся в нем компонентов (сукцината натрия, никотинамида, рибоксина и рибофлавина мононуклеотида), может быть рекомендован для дальнейшей апробации в комплексной терапии ИБС.
Проведенная нами в последующем сравнительная оценка состояния липопероксидации в экспериментах с использованием неотона в динамике ишемии миокарда позволила выявить новые биологические эффекты этого препарата: подавление чрезмерной интенсификации липопероксидации в ишемизированном миокарде при одновременной реактивации ферментного звена антиоксидантной системы. Так, введение неотона приводило к выраженному снижению содержания МДА в гомогенатах миокарда и сыворотке крови (р<0.001) спустя 60 мин с момента развития ишемии. Уровень ДК в крови не изменялся ни в одном из наблюдений (р<0.001). В то же время возрастали активность СОД (р<0.001) и каталазы (р<0.001), уровень восстановленного глутатиона (р<0.001) в гомогенатах миокарда. Активность СОД (р<0.001) и каталазы (р<0.001) сыворотки крови на фоне введения неотона не отличались от таковых показателей групп животных с ишемией миокарда без медикаментозной коррекции, превосходя показатели групп интактных животных. При этом уровень восстановленного глутатиона сыворотки крови заметно возрастал (р<0.001).
Аналогичные свойства антиоксиданта неотон проявлял и при более продолжительной ишемии миокарда (72 часа с момента развития ишемии, при 3-хкратном внутривенном введении препарата). Под влиянием неотона уровень МДА в гомогенатах миокарда заметно снижался (р<0.001), активность СОД (р<0.001) и уровень восстановленного глутатиона (р<0.001) возрастали по отношению к соответствующим показателям группы ишемизированных животных без медикаментозной коррекции. Одновременно снижалось содержание МДА (р<0.001) в сыворотке крови, возрастали активность СОД (р<0.01), каталазы (р<0.05), уровень восстановленного глутатиона (р<0.05) в сыворотке крови по отношению к аналогичным показателям группы сравнения без введения неотона.
Таким образом, результаты проведенных исследований свидетельствуют о развитии положительных метаболических эффектов в ишемизированном миокарде под влиянием неотона, обусловленных реактивацией ферментного звена антиоксидантной системы гомогенатов миокарда и сыворотки крови.
Проведенные наблюдения позволили заключить следующее:
- 1. Выявлена принципиальная возможность подавления чрезмерной интенсификации процессов липопероксидации в ишемизированном миокарде на фоне применения неотона.
- 2. Неотон (экзогенный креатинфосфат) не только является донатором макроэргических фосфатных связей, но и обладает способностью обеспечивать в определенной степени реактивацию важнейших ферментов антиоксидантной системы - СОД и каталазы, увеличивать содержание восстановленного глутатиона, препятствовать чрезмерному накоплению МДА в крови и миокарде, подобно цитофлавину.