
Научная электронная библиотека
Монографии, изданные в издательстве Российской Академии Естествознания

ГНЕЗДНАЯ АЛОПЕЦИЯ: ЛИНИКО-ГЕНЕТИЧЕСКИЕ АСПЕКТЫ И МИКРОЭЛЕМЕНТНЫЙ СТАТУС ПАЦИЕНТОВ
Николаева Т. В., Воронина Л. Г., Сетко Н. П., Пострелко М. Д.,
3. МИКРОЭЛЕМЕНТНЫЙ СТАТУС ПАЦИЕНТОВ С ГНЕЗДНОЙ АЛОПЕЦИЕЙ. ВЛИЯНИЕ ОТДЕЛЬНЫХ МИКРОЭЛЕМЕНТОВ НА РИСК РАЗВИТИЯ ГНЕЗДНОЙ АЛОПЕЦИИ ПО ДАННЫМ МАТЕМАТИЧЕСКОГО МОДЕЛИРОВАНИЯ
Результаты исследований, посвященных изучению возможной роли дисбаланса микроэлементов, представленные в ряде работ [25, 29], часто не согласуются между собой. S. Namkoong (2013), отмечая противоречивость данных о нарушении микроэлементного обмена у пациентов с ГА, считает необходимым проведение дополнительных исследований для определения корреляций между клиническим статусом, минеральным анализом волос и образцов крови пациентов.
Исследование микроэлементного обмена у пациентов с ГА проведено на основании оценки содержания 11 микроэлементов в двух биосубстратах – цельной крови и волосах у 100 пациентов с ГА и 100 здоровых лиц, составивших группу сравнения. Анализ данных табл. 2 показал, что у пациентов с ГА содержание цинка в крови было в 1,3 раза ниже (p = 0,002), чем у лиц группы сравнения. Учитывая патогенез ГА можно предположить, что синтезируемые клетками интра- и перифолликулярного воспалительного инфильтрата, кератиноцитами и меланоцитами волосяного фолликула провоспалительные цитокины ФНО-α, ИФН-γ, ИЛ-1β, ИЛ-6 проявляют системные эффекты [11], оказывающие воздействие на обмен микроэлементов. Эти цитокины подавляют печеночный синтез альбумина, приводят к ослаблению связи цинка с этим белком-переносчиком, приводят к запасанию цинка в гепатоцитах. Кроме того, ИЛ-1β, ИЛ-6,
ФНО-α активируют синтез металлотионеинов 1 и 2 (МТ1, МТ2) в печени и МТ4 в кератиноцитах приводят к внутриклеточному запасанию цинка и, вероятно, к истощению метаболически активного пула Zn2+ в крови.
При этом поступающие в клетки ионы Zn2+ расходуются в реакциях синтеза цитоплазматической Cu/Zn-SOD [79], активации глутатиона и каталаз [41] и в ряде других компенсаторных процессов, активирующихся в условиях воспаления. Реализация описанных механизмов приводит к относительной по сравнению со здоровыми лицами гипоцинкемии, наблюдаемой у пациентов с ГА, при отсутствии накопления цинка в волосах пациентов, где его содержание статистически значимо не отличается от контрольной группы.
Таблица 2
Показатели содержания микроэлементов
в биосредах пациентов с гнездной алопецией и лиц группы сравнения
|
Микроэлементы |
Кровь (мг/л) |
Волосы (мкг/г) |
||||
|
Группа пациентов |
Группа |
p-уровень |
Группа пациентов |
Группа сравнения |
p-уровень |
|
|
Zn |
2,99 [2,3–3,79] |
3,8 [2,73–4,56] |
0,002* |
63,75 [44,3–70,4] |
67,59 [43,1–73,55] |
0,25 |
|
Fe |
123,9 [77,8–175,3] |
162,9 [111,5–202,6] |
0,002* |
30,8 [19,9–44,8] |
14,29 [11,75–21,2] |
0,0001** |
|
Cu |
0,54 [0,25–0,88] |
0,46 [0,27–0,79] |
0,45 |
7,15 [3,96–11,2] |
5,16 [3,28–6,6] |
0,002* |
|
Co |
0,02 [0,008–0,05] |
0,04 [0,02–0,07] |
0,004* |
0,11 [0,05–0,23] |
0,11 [0,08–0,26] |
0,14 |
|
Cr |
0,14 [0,05–0,29] |
0,16 [0,07–0,31] |
0,37 |
1,44 [1,04–2,07] |
1,13 [0,78–1,58] |
0,007* |
|
Mn |
0,22 [0,18–0,26] |
0,22 [0,19–0,32] |
0,11 |
1,41 [1,03–1,6] |
1,16 [0,92–1,79] |
0,21 |
|
Ni |
0,08 [0,04–0,13] |
0,08 [0,05–0,14] |
0,47 |
0,67 [0,48–0,87] |
0,44 [0,25–0,69] |
0,001* |
|
Sr |
0,31 [0,06–0,53] |
0,43 [0,14–0,57] |
0,14 |
1,32 [0,62–2,04] |
1,45 [0,62–2,37] |
0,92 |
|
Bi |
0,02 [0,007–0,06] |
0,04 [0,02–0,09] |
0,006* |
0,05 [0,02–0,22] |
0,04 [0,01–0,11] |
0,41 |
|
Cd |
0,006 [0,002–0,01] |
0,007 [0,003–0,01] |
0,32 |
0,02 [0,01–0,06] |
0,02 [0,007–0,04] |
0,3 |
|
Pb |
0,07 [0,03–0,11] |
0,08 [0,04–0,18] |
0,14 |
0,31 [0,06–0,51] |
0,14 [0,07–0,49] |
0,5 |
Примечание. * – статистическая значимость различий с контрольной группой при уровне р < 0,01; ** – статистическая значимость различий с контрольной группой при уровне р < 0,001.
Провоспалительные цитокины, синтезируемые клеточным инфильтатом в очагах ГА, модулируя синтез печеночных ферментов, вероятно, нарушают гомеостаз железа. Установлено, что уровень железа в крови пациентов был в 1,3 раза ниже, по сравнению со здоровыми лицами (р = 0,002). Наблюдаемая в группе пациентов гипоферремия может быть обусловлена ИЛ-6-индуцированным увеличением синтеза гепсидина гепатоцитами, который снижает абсорбцию железа энтероцитами и препятствует выходу этого микроэлемента из макрофагов [65].
ИЛ-1β-стимулированная выработка лактоферрина гепатоцитами дополнительно приводит к связыванию сывороточного железа, его транспорту в клетки и депонированию с ферритином [65], приводя к внутриклеточному накоплению железа. Указанные механизмы объясняют низкий по сравнению с контрольной группой уровень железа в крови пациентов с ГА, и относительно высокое его содержание в волосах пациентов, превышающее в 2,2 раза концентрацию этого микроэлемента у здоровых лиц группы сравнения (p = 0,0001). Важно отметить, что гипоферремия у больных ГА не сопровождается снижением уровня гемоглобина. Это объясняется тем, что при атомно-абсорбционной спектрофотометрии, использованной в настоящем исследовании, определяется уровень железа в цельной крови без учета валентности химического элемента и соединений, в которые входит этот элемент [17], поэтому гипоферремия отражает содержание железа в совокупности циркулирующих в крови железосодержащих транспортных белков и ферментов.
У пациентов с ГА выявлено снижение концентрации кобальта в крови, содержание которого было в 2 раза ниже по сравнению со здоровыми лицами (р = 0,004). Снижение содержания кобальта, вероятно,
объясняется его потреблением в качестве кофактора в реакциях биосинтеза глутатиона [53] и кофактора глутатионпероксидазы [56], необходимых для реализации антиоксидантной защиты в условиях окислительного стресса. При этом снижения содержания кобальта в волосах не отмечается. Это обстоятельство может объясняться тем, что в условиях дефицита железа происходит увеличение абсорбции кобальта [55] и восполнение потребности в нем организма.
У пациентов с ГА выявлено снижение содержания висмута в крови, его уровень был в 2 раза ниже, чем у лиц группы сравнения (р = 0,006). Снижение концентрации висмута невозможно объяснить с точки зрения биологической целесообразности в силу отсутствия описанного участия этого элемента в метаболических процессах. Вероятно, снижение содержания висмута в крови является следствием описанных выше изменений обмена эссенциальных микроэлементов. Известно, что высвободившиеся из связи с альбумином ионы Zn2+, индуцируют синтез МТ в печени [71], при этом Bi3+, отличаясь высоким сродством к МТ, превышающим аффинитет к нему таких металлов, как Zn2+ и Cd2+ [44], связывается с ним и транспортируется из крови в ткани. Так, в волосах пациентов отмечается тенденция к накоплению этого металла, содержание которого на 25 % выше по сравнению с уровнем Bi3 + у здоровых лиц.
Увеличение синтеза трансферрина в печени, которое является компенсаторной реакцией на снижение уровня железа в крови [2], может выступить еще одним возможным механизмом снижения концентрации Bi в крови. Трансферрин, выступая в качестве основного переносчика железа к клеткам, выполняет функцию транспортера других металлов, в частности Bi3+, Cr3+ и Ni2+ к тканям [82].
Сравнительный анализ микроэлементного состава волос показал, что у больных ГА уровень Ni2+ в 1,5 раза превысил таковой у здоровых лиц группы сравнения (р = 0,001) при отсутствии различий в содержании этого микроэлемента в крови. Известно, что основной транспортной системой, доставляющей ионы Ni2+ в клетки является транспортер двухвалентных металлов 1 типа (DMT1) [36]. Вследствие гипоферремии усиливается синтез DMT1 в энтероцитах [61], что может приводить к усиленной абсорбции ионов Ni2+ [32], поступающего из окружающей среды в условиях техногенного загрязнения. Увеличение в условиях воспаления печеночного синтеза белков, транспортирующих металлы, таких как МТ1, МТ2 [43], трансферрина [50], приводит к эффективному перемещению абсорбированного Ni2+ из русла крови в ткани, где накапливаясь, он, возможно, реализует ряд токсических эффектов.
Аналогичные изменения отмечены в показателях содержания Cr3+ в биосредах пациентов и лиц группы сравнения. Установлено, что содержание Cr3+ в волосах пациентов в 1,3 раза превышает аналогичный показатель у здоровых людей (р = 0,007). Механизм избыточного накопления Cr3+ в волосах пациентов, вероятно, связан с увеличением его абсорбции на фоне дефицита Zn2+ и Fe2+ [19] с последующим переносом в ткани трансферрином [50]. Хром также является металлом-загрязнителем. Баланс цинка и железа в организме, вероятно, препятствует поступлению металлов-загрязнителей в организм человека.
При оценке микроэлементного состава волос пациентов установлено увеличение в их структуре содержания меди, уровень которой в 1,4 раза превысил таковой в волосах здоровых людей (р = 0,002). Возможно, это является следствием стимулирующего влияния провоспалительных цитокинов ИЛ-1β и ИЛ-6, которые активируют синтез церулоплазмина гепатоцитами и транспорт меди в ткани [80]. При этом содержание этого микроэлемента в крови не изменяется, что, вероятно, обусловлено поглощением меди в количестве, превышающем метаболические потребности организма [38].
Ряд исследователей считает более объективным параметром не собственно показатели содержания микроэлементов в биосубстратах, подверженные значительным индивидуальным колебаниям [64], а соотношения между ними [39]. Известно, что отдельные показатели соотношения между микроэлементами с про- и антиоксидантными свойствами могут являться индикаторами антиоксидантного статуса, в частности, показатели Zn/Cu, Cu/Mn, Co/Ni в крови [28]. Кроме того, показатель Cu/Zn в крови считается одним из достоверных маркеров воспаления [26]. Учитывая, что ГА сопровождается нарушением антиокислительного гомеостаза [30], на который в свою очередь оказывает влияние микроэлементный статус [62] проведен анализ перечисленных показателей соотношения, представленных в табл. 3.
Таблица 3
Показатели соотношения содержания микроэлементов
в крови пациентов с гнездной алопецией (1) и лиц группы сравнения (2)
|
Соотношения микроэлементов |
Группа |
Показатели соотношения |
р-уровень |
|
|
Количественный |
Me (Q25–Q75) |
|||
|
Cu/Zn |
1 |
1:3,70 |
0,17 (0,08–0,34) |
0,021* |
|
2 |
1:6,67 |
0,11 (0,08–0,21) |
||
|
Zn/Cu |
1 |
10,16:1 |
5,91 (2,92–11,94) |
0,021* |
|
2 |
11,36:1 |
8,97 (4,66–12,0) |
||
|
Cu/Mn |
1 |
3,13:1 |
2,42 (1,46–4,29) |
0,021* |
|
2 |
2,27:1 |
1,70 (1,1–3,06) |
||
|
Co/Ni |
1 |
1:1,44 |
0,3 (0,12–0,76) |
0,206 |
|
2 |
1:1,39 |
0,42 (0,2–0,89) |
||
Примечание. Коэффициент значим на уровне: p < 0,05 (*); p < 0,01 (**).
Анализ данных табл. 3 показал, что медиана показателя соотношения Cu/Zn у пациентов с ГА в 1,5 раза выше, чем аналогичный показатель у лиц группы сравнения (р = 0,021), что является системным признаком наличия воспалительного процесса в организме пациентов с ГА. Соответственно показатель соотношения Zn/Cu, отражающий эффективность работы антиокислительных систем [16], у больных ГА в 1,5 раза ниже, чем у здоровых людей (р = 0,021). Установлено, что, несмотря на отсутствие статистически значимых различий по содержанию в крови Mn и Cu, показатель соотношения Cu/Mn у больных ГА в 1,4 раза выше такового у здоровых лиц (р = 0,021). Вместе с тем, показатели соотношения Co/Ni у пациентов и здоровых лиц не отличались (р = 0,206), вследствие отсутствия различий показателей концентрации Ni в крови больных ГА и здоровых лиц группы сравнения.
Учитывая преимущественное биологическое действие микроэлементов, в частности, прооксидантную активность Cu [51] и антиоксидантное влияние Zn и Mn [24], можно предположить, что у пациентов с ГА имеет место активация прооксидантных реакций и неэффективность работы антиоксидантных систем [16].
На основе проведенного анализа предположено, что описанные изменения микроэлементного обмена у пациентов с ГА являются результатом как имеющегося аутоиммунного воспалительного процесса, так и поступления металлов-загрязнителей из окружающей среды. Вместе с тем формирующийся дисбаланс химических элементов неизбежно влияет на течение патологического процесса, поддерживая его. Так, ранняя фаза ГА характеризуется преждевременным переходом анагенового фолликула в стадию катагена [60], в то же время дефицит железа и цинка также обладает катаген-индуцирующим влиянием [68]. Повышение показателя соотношения Cu/Zn и снижение Zn/Cu, Cu/Mn являются маркерами низкой эффективности антиоксидантной защиты, свидетельствующие об активации процессов свободнорадикального окисления, которые не только могут поддерживать воспаление [57], но и способствовать прогрессированию аутоиммунного процесса путем увеличения синтеза ИЛ-6 [52]. Адаптивный ответ на оксидативный стресс, заключающийся в увеличении синтеза глутатиона и пероксидазы, требующий в качестве кофактора ионы Co2+, вероятно, приводит к снижению содержания его в крови пациентов с ГА.
Проведенный выше анализ показал, что микроэлементный статус организма представляет собой результат сложного взаимодействия целого ряда отдельных микроэлементов, характер которого изменяется при нарушении гомеостаза. Микроэлементный обмен, представляя собой процесс, описываемый множеством признаков, требует применения многомерных методов анализа, «которые дают оценку с учетом всех или большинства признаков» [6] одновременно. Применение логистического регрессионного анализа позволило оценить связь между многими показателями микроэлементного статуса, являющимися независимыми переменными и зависимой бинарной переменной, принимающей одно из двух значений, в частности отсутствие или наличие ГА у обследуемого, оценить вклад отдельных микроэлементов в патогенез ГА и предсказать вероятность болезни в зависимости от значений показателей микроэлементного обмена. Важно отметить, что представленная модель не несет диагностической ценности, поскольку диагностика ГА в подавляющем большинстве случаев не вызывает затруднений. Однако моделирование ГА на основании данных многоэлементного анализа позволяет выявить значимые для патогенеза заболевания микроэлементы, получить новые данные об их влиянии на болезнь, что представляет не только теоретический, но и практический интерес.
Построение оптимальной модели проводилось путем пошагового исключения из первоначальной модели наименее значимых признаков. В результате ряда преобразований в модели остались 8 показателей с уровнем значимости р < 0,05. К ним относятся показатели Со, Cu, Mn в крови и Cu, Fe, Cr, Zn в волосах. Значение статистики Вальда Wald chi2(7) = 28,88, соответствующее p-значение p = 0,0003 и коэффициент детерминации Pseudo R2 = 0,3272 построенной логит-модели доказывают, что она статистически значима и может использоваться для прогнозирования принадлежности участников исследования к группе пациентов или к группе сравнения. Результаты построения логит-модели с пошаговым исключением переменных представлены в табл. 4.
На основе проведенного логистического регрессионного анализа построена математическая модель ГА, описываемая формулой (1). Она представляет собой зависимость бинарной переменной
от совокупности независимых признаков – восьми показателей микроэлементного обмена.
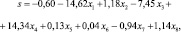 (1)
(1)
|
где s – |
показатель экспоненты; |
|
–0,60 – |
свободный член, не имеющий клинической интерпретации; |
|
х1 – |
показатель содержания Co в крови; |
|
х2 – |
показатель содержания Cu в крови; |
|
х3 – |
показатель содержания Mn в крови; |
|
х4 – |
показатель содержания Cd в волосах; |
|
х5 – |
показатель содержания Cu в волосах; |
|
х6 – |
показатель содержания Fe в волосах; |
|
х7 – |
показатель содержания Mn в волосах; |
|
х8 – |
показатель содержания Cr в волосах. |
Таблица 4
Коэффициенты логистической регрессионной модели
прогнозирования гнездной алопеции
на основании 8 показателей микроэлементного статуса
|
Биосреда |
Микроэлемент |
Обозначение |
Коэффициент |
Стандартная ошибка |
p-уровень |
|
Кровь |
Co |
x1 |
–14,62 |
6,742 |
0,030* |
|
Cu |
x2 |
1,18 |
0,536 |
0,028* |
|
|
Mn |
x3 |
–7,45 |
1,921 |
0,000*** |
|
|
Волосы |
Cd |
x4 |
14,34 |
5,487 |
0,009** |
|
Cu |
x5 |
0,13 |
0,060 |
0,026* |
|
|
Fe |
x6 |
0,04 |
0,015 |
0,003** |
|
|
Mn |
x7 |
–0,94 |
0,378 |
0,012* |
|
|
Cr |
x8 |
1,14 |
0,417 |
0,006** |
|
|
Свободный член |
–0,60 |
0,905 |
0,506 |
||
Примечание. Коэффициент значим на уровне: p < 0,05 (*); p < 0,01 (**); p < 0,001 (***).
Вероятность принадлежности участников исследования к группе пациентов, страдающих ГА, (y) рассчитана по формуле бинарной логистической регрессии, имеющей вид:
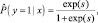 (2)
(2)
|
где s – |
показатель экспоненты, рассчитывающийся по формуле (1); |
|
|
вероятность. |
В том случае, если вероятность  менее 0,5, то участник исследования относится к группе сравнения, если более 0,5 – к группе пациентов, страдающих ГА.
менее 0,5, то участник исследования относится к группе сравнения, если более 0,5 – к группе пациентов, страдающих ГА.
Для проверки предсказательной способности представленной модели были проведены следующие исследования.
Пример 1.
Показатели микроэлементного статуса пациентки 30 лет, страдающей очаговой формой ГА:
показатель содержания Co в крови (х1) – 0,067 мг/л;
показатель содержания Cu в крови (х2) – 0,25 мг/л;
показатель содержания Mn в крови (х3) – 0,147 мг/л;
показатель содержания Cd в волосах (х4) – 0,01 мкг/г;
показатель содержания Cu в волосах (х5) – 3,74 мкг/г;
показатель содержания Fe в волосах (х6) – 56,02 мкг/г;
показатель содержания Mn в волосах (х7) – 1,51 мкг/г;
показатель содержания Cr в волосах (х8) – 1,89 мкг/г.
Вычислен показатель экспоненты (s), путем подставления указанных концентраций микроэлементов в формулу (1):
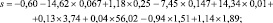
s = 1,22591.
Рассчитано значение экспоненты с использованием программы «Microsoft Excel 2003»:
exp(1,22591) = 3,407265.
Вычислена вероятность  по формуле (2):
по формуле (2):
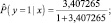
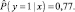
С учетом полученного значения вероятности, которое больше 0,5, обследуемая страдает ГА и относится к группе пациентов.
Чувствительность модели, рассчитанная как отношение истинно-положительных результатов к общему количеству пациентов, составила 89 %. Специфичность, являющаяся отношением истинно-отрицательных результатов к числу лиц группы сравнения, равна 74 %. Для численного выражения качества модели использован показатель площади под ROC-кривой AUC (Area Under Curve), которая в данном случае составляет 0,8671. Согласно экспертной шкале для значений AUC, интервал от 0,8 до 0,9 соответствует очень хорошему качеству модели [7]. Проведенный логистический регрессионный анализ показал, что значимое влияние на вероятность наличия ГА оказывает содержание Co, Cu, Mn в крови и Cd, Cu, Fe, Mn и Cr в волосах. Интерпретировать влияние указанных микроэлементов позволяют знаки коэффициентов логит-модели, описанной формулой (1). Положительный коэффициент свидетельствует о том, что его возрастание увеличивает вероятность ГА, а рост коэффициента с отрицательным знаком, напротив, будет способствовать снижению вероятности заболевания [14]. Анализ данных, представленных в табл. 3, показывает, что увеличение показателей Co и Mn в крови и Mn в волосах, будут снижать вероятность ГА, а увеличение содержания Cu в крови и уровней Cd, Cu, Fe и Cr в волосах – ее увеличивать. С учетом описанных выше возникающих изменений микроэлементного обмена в организме пациентов с ГА представленная логит-модель биологически адекватна. Во-первых, полученные результаты не противоречат данным проведенного сравнительного анализа и выявленным изменениям в организме пациентов с ГА. Во-вторых, отсутствуют противоречия с выполняемой биологической ролью вошедших в логит-модель микроэлементов. В представленной модели антиоксидантной роли Co и Mn противопоставлены прооксидантные и токсичные эффекты Cd, Cu, Fe и Cr.
 –
–